شروع کارآزمایی بالینی یک داروی جدید برای موارد شدید کووید-19
به گزارش انجمن وردپرس، پژوهشگران آمریکایی کارآزمایی بالینی با یک داروی جدید- یک آنتی بادی مونوکلونال یا پادتن تک دودمانی- را برای موارد کووید-19 با درگیری شدید ریوی غاز می نمایند.
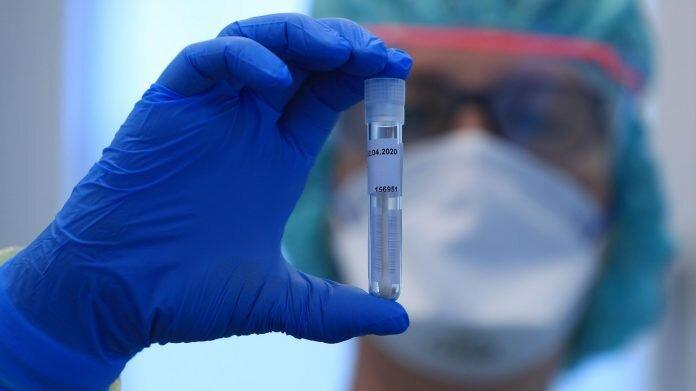
به گزارش انجمن وردپرس به نقل از هلث دی نیوز این کارآزمایی بالینی با داروی جیمسیلوماب (gimsilumab) در دانشگاه تمپل آمریکا بر روی موارد شدید بیماری کووید-19 که عفونت در آنها ریه ها را از کار انداخته است، انجام خواهد شد.
موسسه های پژوهشی دیگر نیز از آنتی بادی های خون بیماران بهبودیافته برای درمان موارد شدید کووید-19 استفاده نموده اند. این کارآزمایی بالینی جدید با این آنالیز ها متفاوت است، چرا که جیمسیلوماب آنتی بادی یا پادتنی است که در آزمایشگاه ساخته شده است و در صورت ثابت شدن تاثیربخشی می توان آن را فراوری انبوه کرد.
هدف اولیه این آنالیز اندازه گیری میزان مرگ ومیر در میان تا 270 بیمار با بیماری ثابت شده کووید-19 است. نیمی از بیماران به طور تصادفی انتخاب می شوند تا این دارو را دریافت نمایند و به نیمی دیگر دارونما (پلاسبو) داده می گردد. این کارآزمایی همچنین تاثیر این دارو را بر میزان احتیاج بیماران به استفاده از دستگاه تنفس مصنوعی و زمان گذرانده شده در بخش مراقبت های ویژه آنالیز خواهد نمود.
آنتی بادی های مونوکلونال یا پادتن های تک دودمانی مولکول های فراوریشده در آزمایشگاه هستند که طوری طراحی می شوند که به یک آنتی ژن یا پادگن خاص متصل شوند و آن را خنثی نمایند.
داروی جیمسیلوماب فاکتور تحریک نماینده کلنی گرانولوسیبت-ماکروفاژ (GM-CSF) را هدف قرار می دهد که تصور می گردد عاملی اصلی در التهاب بیش از حد ریه ها باشد.
آنالیز های اولیه نشان داده اند که GM-CSF ممکن است در بدتر شدن بالینی بیماران کووید-19 نقش داشته باشد.دستگاه ایمنی بدن سیاری از بیماران کووید-19 پاسخ بسیار شدیدی در برابر عفونت ویروسی ایجاد می نماید که خودش به ریه ها آسیب می زند و ممکن است به نشانگاه زجر تنفسی حاد (ARDS) منجر گردد.
ARDS که با آسیب التهابی ریه ها همراه است به سفت شدن ریه ها و کاهش توانایی اکسیژن رسانی ها آنها می انجامد و احتیاج به اتصال به دستگاه تنفس مصنوعی را ایجاد می نماید. این نشانگان میزان مرگ ومیری تا بالای 40 درصد دارد.
جیمسیلوماب در آنالیز های غیر بالینی متعدد و نیز دو آنالیز بالینی قبلی از جمله یک کازآزمایی بالینی چهار هفته ای مرحله یک آزمایش شده است. این آنالیز ها نشان دهنده بی خطر بودن و تحمل پذیری این دارو بر اساس داده های گردآوری شده بوده اند.
منبع: همشهری آنلاین